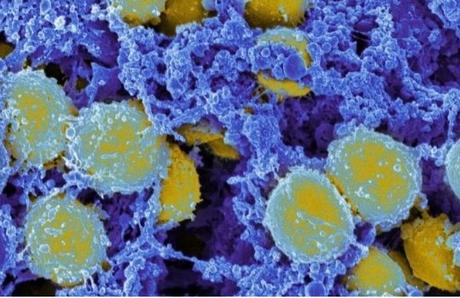
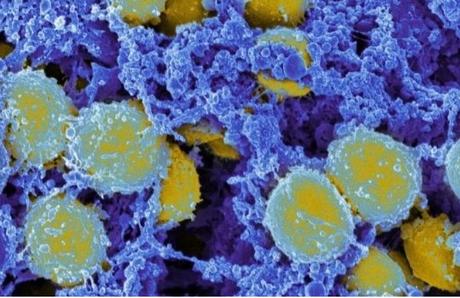
Ces chercheurs du Vanderbilt University Medical Center viennent de mettre à jour un nouveau mécanisme antibactérien : les neutrophiles et les macrophages, deux acteurs essentiels à la réponse immunitaire innée coopèrent pour capturer et « manger » les bactéries. Ce mécanisme de défense documenté dans la revue Science Advances, inspire de nouvelles stratégies pour lutter contre Staphylococcus aureus et contre d’autres agents bactériens pathogènes .
On savait déjà que les neutrophiles, des cellules immunitaires qui migrent vers les sites d’infection, peuvent s’autodétruire et libérer leur contenu en protéines et en ADN pour générer des « sortes » de filets ou pièges extracellulaires des neutrophiles (NETs pour Neutrophil Extracellular Traps). L’auteur principal, le Dr Eric Skaar, professeur de pathologie, de microbiologie et d’immunologie et directeur du Vanderbilt Institute for Infection, immunologie et inflammation compare ces NETs à « des toiles d’araignées qui immobilisent les bactéries, et les macrophages sont les araignées qui engloutissent et tuent les bactéries ».
L’antibiorésistance, un des grands défis de santé publique
Les bactéries staphylococciques résistantes aux antibiotiques (Staphylococcus aureus résistant à la méticilline- SARM) sont l’une des principales causes d’infections nosocomiales, de cardiopathies infectieuses et d’infections de la peau et des tissus mous.
Les neutrophiles et les macrophages sont 2 types de cellules phagocytaires connus pour ingérer des bactéries et produire des peptides antimicrobiens, des espèces réactives de l’oxygène et d’autres enzymes pour lutter contre les infections. La génération de NETs qui sont le produit d’une forme inflammatoire de la mort cellulaire des neutrophiles appelé « NETosis » est une stratégie antibactérienne des neutrophiles plus récemment découverte : l’ADN neutrophile libéré crée un piège collant qui est également parsemé de peptides antimicrobiens.
La NETose booste aussi les macrophages : l’équipe travaille ici à partir de neutrophiles qui subissent une NETose accrue dans des systèmes modèles animaux et in vitro pour mieux comprendre la fonction biologique des NET. Les chercheurs constatent qu’une augmentation de la NETose n’apporte pas d’efficacité supplémentaire aux neutrophiles isolément. Mais en présence des macrophages, la formation de NET améliore l’activité antibactérienne des macrophages en augmentant la phagocytose des bactéries staphylococciques coincées dans les NET avec des peptides antimicrobiens neutrophiles. En synthèse,
les macrophages disposent alors, en plus leur propre arsenal antibactérien, de celui des neutrophiles.
L’augmentation de la NETose stimule également la destruction par les macrophages d’autres agents pathogènes bactériens, notamment Streptococcus pneumoniae et Pseudomonas aeruginosa. Les résultats suggèrent que la coopération neutrophile / NET-macrophage est un mécanisme de défense immunitaire largement utilisé.
Vers une approche anti-virulence : « Il semble que des agents pathogènes extracellulaires comme le staphylocoque aient développé des enzymes nucléases afin de se frayer un chemin hors de ces NETS et de s’échapper ». En bloquant ces nucléases, les chercheurs émettent l’hypothèse de pouvoir accroître la vulnérabilité des pathogènes à la destruction par les NETs et donc développer une stratégie antibactérienne plus efficace.
« Nous apprenons beaucoup sur les mécanismes de virulence bactérienne et nous pouvons trouver des moyens créatifs de les inhiber. Cependant, les efforts pharmaceutiques actuels se concentrent plutôt sur les médicaments qui tuent directement les bactéries plutôt que sur des médicaments capables d’atténuer leur virulence ».
Source: Science Advances 10 Sep 2021 DOI: 10.1126/sciadv.abj2101 Neutrophil extracellular traps enhance macrophage killing of bacterial pathogens
Plus sur les NETs
Équipe de rédaction SantélogOct 26, 2021Équipe de rédaction Santélog
