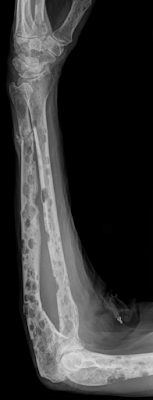
Ostéolyses multiples et fracture de l'ulna dans un cas de plasmocytome (myélome multiple).
Source iconographique et légendaire:https://fr.wikipedia.org/wiki/Myélome
Dans l'analyse principale de l'essai de phase 3 MAIA (suivi médian de 28,0 mois), une amélioration significative de la survie sans progression a été observée avec le daratumumab plus lénalidomide et dexaméthasone versus lénalidomide et dexaméthasone seuls chez les patients non éligibles à la transplantation le myélome multiple. Nous rapportons ici les résultats d'efficacité et d'innocuité mis à jour à partir d'une analyse intermédiaire prédéfinie pour la survie globale.
MAIA est un essai de phase 3, multicentrique, randomisé, ouvert et en cours qui a recruté des patients dans 176 hôpitaux situés dans 14 pays d'Amérique du Nord, d'Europe, du Moyen-Orient et de la région Asie-Pacifique. Les patients éligibles étaient âgés de 18 ans ou plus, avaient un myélome multiple nouvellement diagnostiqué, avaient un score de performance de l'Eastern Cooperative Oncology Group de 0 à 2 et n'étaient pas éligibles pour une chimiothérapie à haute dose avec autogreffe de cellules souches en raison de leur âge (≥ 65 ans) ou des comorbidités. Les patients ont été assignés au hasard (1:1) à l'aide de blocs permutés au hasard (taille de bloc 4) par un système de réponse Web interactif pour recevoir des cycles de 28 jours de daratumumab par voie intraveineuse (16 mg/kg, une fois par semaine pendant les cycles 1 à 2, une fois tous les 2 semaines dans les cycles 3 à 6, et une fois toutes les 4 semaines par la suite) plus lénalidomide par voie orale (25 mg aux jours 1 à 21 de chaque cycle) et dexaméthasone par voie orale (40 mg aux jours 1, 8, 15 et 22 de chaque cycle ; groupe daratumumab) ou lénalidomide et dexaméthasone seuls (groupe témoin). La randomisation a été stratifiée selon le stade de la maladie du système international de stadification, la région géographique et l'âge. Ni les patients ni les investigateurs n'étaient masqués à l'attribution du traitement. Le critère d'évaluation principal était la survie sans progression, qui a été évaluée de manière centralisée, et un critère d'évaluation secondaire était la survie globale (tous deux évalués dans la population en intention de traiter). La population de tolérance comprenait des patients ayant reçu au moins une dose du traitement à l'étude. Les résultats présentés ici proviennent d'une analyse intermédiaire prédéfinie pour la survie globale, pour laquelle la limite d'arrêt prédéfinie était p = 0,0414.
Entre le 18 mars 2015 et le 15 janvier 2017, 952 patients ont été évalués pour l'éligibilité, dont 737 patients ont été inclus et assignés au hasard au groupe daratumumab (n=368) ou au groupe témoin (n=369). À un suivi médian de 56,2 mois (Intervalle Interquartile [IQR] 52,7–59,9), la survie médiane sans progression n'a pas été atteinte (Intervalle de Confiance [IC] 95 % 54,8–non atteint) dans le groupe daratumumab versus34,4 mois (29,6-39,2) dans le groupe témoin (hazard ratio [HR] 0,53 [IC 95 % 0,43-0,66] ; p<0,0001). La survie globale médiane n'a été atteinte dans aucun des groupes (groupe daratumumab, IC à 95 % non atteint – non atteint ; groupe témoin, IC à 95 % 55,7 – non atteint ; HR 0,68 [IC 95 % 0,53-0,86] ; p=0,0013). Les événements indésirables survenus pendant le traitement de grade 3 ou plus les plus fréquents (> 15 %) étaient la neutropénie (197 [54 %] patients dans le groupe daratumumab contre 135 [37 %] patients dans le groupe témoin), la pneumonie (70 [19 %] vs 39 [11%]), anémie (61 [17%] vs 79 [22%]) et lymphopénie (60 [16%] vs 41 [11%]). Des événements indésirables graves sont survenus chez 281 (77 %) patients du groupe daratumumab et 257 (70 %) patients du groupe témoin. Des décès liés au traitement sont survenus chez 13 (4 %) patients du groupe daratumumab et dix (3 %) patients du groupe témoin.
Le daratumumab associé au lénalidomide et à la dexaméthasone a augmenté la survie globale et la survie sans progression chez les patients non éligibles à une greffe de cellules souches atteints d'un myélome multiple nouvellement diagnostiqué. Il n'y a eu aucun nouveau problème de sécurité. Nos résultats soutiennent l'utilisation de première ligne du daratumumab plus lénalidomide et dexaméthasone pour les patients atteints de myélome multiple qui ne sont pas éligibles pour une transplantation. Prof Thierry Facon, MD, et al, dans The Lancet Oncology, publication en ligne en avant-première, 13 octobre 2021
Financement : Janssen Research & Development
Source : The Lancet Online / Préparation post : NZ
