

Ces scientifiques de l’University of North Carolina qui viennent de cartographier l'infection par le SRAS-CoV-2 dans les cellules de la cavité nasale, des bronches et des poumons ajoutent à la preuve de l’efficacité voire de la nécessité du port d'un masque pour limiter la transmission de COVID-19. Ces travaux, présentés dans la revue Cell confirment en effet que le coronavirus SRAS-CoV-2 infecte la d’abord la cavité nasale pour se reproduire très rapidement dans « les cellules du nez » alors que le virus se réplique progressivement moins bien dans les cellules situées plus bas dans les voies respiratoires, y compris dans les poumons.
Tout commence dans le nez, avait déjà expliqué cette équipe de l'Université de Cincinnati qui confirmait déjà une charge virale élevée dans les sécrétions nasales. Ces nouveaux résultats suggèrent que le virus a en effet tendance à s'établir fermement d'abord dans la cavité nasale, mais peut être ensuite « aspiré » dans les poumons, où il peut provoquer une maladie plus grave, dont une pneumonie mortelle.
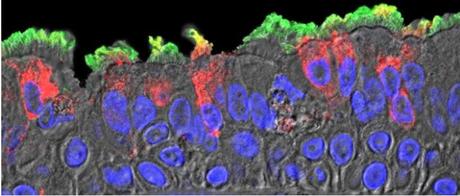
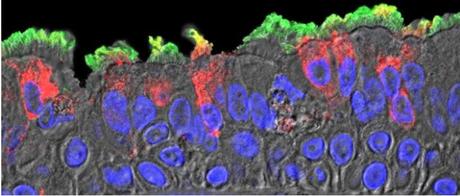
Le nez est le site initial d’infection, à partir duquel le virus peut déclencher l'infection pulmonaire
« l'utilisation généralisée de masques pour protéger les voies nasales, ainsi que toutes les stratégies thérapeutiques qui réduisent le risque de virus dans le nez, telles que l'irrigation nasale ou les vaporisateurs nasaux antiviraux, sont bénéfiques », expliquent les auteurs, le Dr Richard Boucher, professeur de médecine et le Dr Ralph Baric, professeur d'épidémiologie.
L’équipe identifie également le mécanisme qui régule la progression et la sévérité de la maladie après une infection par le SRAS-CoV-2, soit comment le coronavirus infecte les cellules des voies respiratoires et comment il pénètre dans les poumons chez les patients qui développent une pneumonie. Dans une série d'expériences de laboratoire, les chercheurs ont regardé comment plusieurs souches infectent les cellules cultivées de différentes zones de l’appareil respiratoire. C’est ainsi qu’ils constatent une infectiosité relativement élevée du SRAS-CoV-2 dans les cellules tapissant les voies nasales, puis une infectiosité moindre dans les cellules tapissant la gorge et les bronches, et, enfin une infectiosité relativement faible dans les cellules pulmonaires.
La densité du récepteur de surface cellulaire ACE2 que le virus utilise pour pénétrer dans les cellules est d’ailleurs corrélée à cette infectiosité qui décline progressivement : ACE2 est plus abondant sur les cellules de la muqueuse nasale et moins abondant sur la surface des cellules des voies respiratoires inférieures. Cette différence contribue à expliquer pourquoi les cellules de la muqueuse nasale des voies aériennes supérieures sont plus sensibles à l'infection.
Sur 2 protéines de clivage favorisant l’infection : d'autres expériences portent sur TMPRSS2 et la furine, 2 enzymes de clivage des protéines trouvées sur de nombreuses cellules humaines. On pense que le SRAS-CoV-2 utilise ces deux enzymes pour remodeler les protéines virales clés et pénétrer dans les cellules humaines. Les expériences confirment que lorsque ces enzymes humaines sont plus abondantes, la capacité de SARS-CoV-2 à infecter les cellules et à se reproduire est considérablement accrue.
L'identification des cellules infectées : les chercheurs constatent également que le virus peut infecter les cellules tapissant les voies respiratoires appelées cellules épithéliales et, dans une mesure limitée, les cellules pulmonaires « pneumocytes » qui aident à transférer l'oxygène inhalé dans la circulation sanguine. Mais le SRAS-CoV-2 n'infecte presque aucune autre cellule des voies respiratoires. Curieusement, le virus n’infecte pas les cellules « club » ou « clara cells » qui tapissent les voies respiratoires alors que ces cellules expriment à la fois ACE2 et TMPRSS2.
De plus, la sensibilité à l’infection des cellules épithéliales des voies aériennes de différents donneurs humains varie considérablement, ce qui suggère l’existence de facteurs incompris déterminant le cours de l'infection selon les individus.
La cartographie des sites d'infection dans les poumons de plusieurs personnes décédées de COVID-19 confirme l'hypothèse d’une aspiration du contenu nasal dans les poumons pouvant entraîner la pneumonie. Les personnes âgées, obèses et diabétiques sont plus sujettes à ce type d’aspiration, en particulier la nuit, suggèrent les chercheurs.
Le développement possible d’une immunité croisée modérée : l'équipe constate que les anticorps capables de neutraliser le SRAS et le MERS ne sont pas capables de neutraliser le SRAS-CoV-2. Cependant, elle confirme une réactivité croisée à partir des résultats d’analyse du sérum sanguin de 2 patients atteints du SRAS qui révèle, in vitro, une capacité faible mais significative de neutraliser SRAS-CoV-2. Ces données suggèrent la possibilité, chez certains sujets seulement, d’une immunité croisée au moins partielle contre le SRAS-CoV-2.
Des conclusions précieuses à la fois pour la prévention de l’infection mais aussi pour le ciblage des futurs traitements et vaccins anti-COVID-19.
Source: Cell 20 mai 2020 DOI : /10.1016/j.cell.2020.05.042 SARS-CoV-2 Reverse Genetics Reveals a Variable Infection Gradient in theRespiratory Tract (Visuel Takanori Asakura, PhD, UNC School of Medicine)
Plus sur COVID-19
Lire aussi : COVID-19 : Pourquoi on ne doit pas mettre le nez dehors
Équipe de rédaction SantélogJuin 3, 2020Rédaction Santé log
