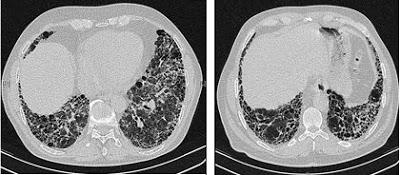
Tomographie à haute résolution du thorax d'un patient atteint de fibrose pulmonaire idiopathique.
Source iconographique et légendaire: https://commons.wikimedia.org/wiki/File:HR_tomography_of_the_chest_of_an_IPF_patient.jpg
L’hétérogénéité de progression de la fibrose pulmonaire idiopathique (FPI) peut refléter la diversité de la pathobiologie sous-jacente ; elle représente quoi qu’il en soit un défi majeur pour ce qui est de la prédiction de la progression clinique ainsi que du bénéfice à tirer du traitement. De précédentes études ont établi que les niveaux mesurés de protéines biomarqueurs peuvent servir de pronostic pour ce qui est de la durée de survie globale des patients atteints de FPI, mais ces données n’ont pas été l’objet de comparaisons entre les cohortes. Notre but était d’utiliser des essais pivot testant le traitement à la pirfenidone pour l’évaluation le pronostic et les propriétés prédictives des biomarqueurs sur plusieurs paramètres, et comment ils sont modulés par un traitement à la pirfenidone.
Nous avons effectué des analyses post-hoc sur cohortes tests et cohortes de réplication à l’aide de données extraites des essais CAPACITY 004, CAPACITY 006, et ASCEND pour ce qui est des protéines plasmatiques CCL13, CCL17, CCL18, CXCL14, COMP, interleukine 13, MMP3, MMP7, ostéopontine, périostine, et YKL40. Les patients éligibles étaient atteints de FPI et recevaient la pirfenidone à raison de 2 403 mg/jour ou le placebo ; les étaient répertoriés dans cohortes CAPACITY (cohorte test) ou ASCEND (replication cohort), étaient âgés de 40-80 ans, et ne présentaient aucun biomarqueur manquant à la ligne de base. Afin d’identifier les biomarqueurs fiables comme indicateurs cliniques de résultats, l’analyse principale était l’association entre les concentrations en biomarqueurs à la ligne de base et le changement absolu exprimé en pourcentage de la capacité vitale forcée prédite (FVC%pred) à 12 mois (CAPACITY week 48, ASCEND week 52) dans le groupe placebo. Les biomarqueurs de la cohorte test satisfaisant aux critères de succès, à savoir une valeur p pronostique inférieure à 0.10 extraite de l’analyse multivariée étaient également mesurés dans la cohorte de réplication. De plus, l’ampleur de l’effet à valeur prédictive (c’est-à-dire, les biomarqueurs qui étaient prédictifs pour ce qui du bénéfice obtenu sous pirfenidone) était définie par la différence entre l’effet du traitement exprimé par la FVC%pred (pirfenidone versus placebo) entre les sous-groupes à biomarqueurs élevés versus les sous-groupes à biomarqueurs faibles à la semaine 48 (cohorte test) ou semaine 52 (cohorte de réplication).
Plusieurs biomarqueurs mesurés à la ligne de base (CCL13, CCL18, COMP, CXCL13, CXL14, périostine, et YKL 40) présentaient une valeur pronostique de progression de la maladie dans les groupes placebo de la cohorte test. Cependant, seul le biomarqueur CCL18 était représentatif d’une valeur pronostique fiable pour ce qui du pourcentage de FVC%pred, à la fois dans la cohorte test (p=0.032) et dans la cohorte de réplication (p=0.004). Le bénéfice d’un traitement par la pirfenidone était consistant, quelle que soit la concentration en biomarqueurs à la ligne de base.
Les concentrations de CCL18 dans le sang représentaient la valeur prédictive la plus consistante de progression de la maladie au sein des cohortes de patients atteints de FPI, avec le potentiel d’apporter des éléments nouveaux en termes de recherche de nouvelles cibles thérapeutiques et dans la conception de nouveaux essais cliniques. Une validation de ces résultats dans le futur, faisant l’objet d’études prospectives, se justifie. Margaret Neighbors, PhD, et al, dans The Lancet Respiratory Medicine, publication en ligne en avant-première, 29 juin 2018
Financement : Genentech Inc
Source : The Lancet Online / Traduction et adaptation : NZ
