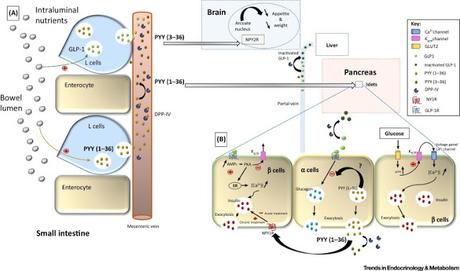
Rôle du PYY dans la régulation du Glucose. (A). A la suite de la prise alimentaire, le PYY (1-36) est sécrété par les cellules L du tractus gastro-intestinal, avant d’être sécrété dans la veine mésentérique. (…). Dans le cerveau, l’intéraction du PYY (3-36) avec le récepteur présynaptique NPY2R - inhibiteur des neurones à Neuropeptide Y (NPY) - soumet à régulation l’effet anorexigène, provoquant une réduction de la prise alimentaire. (…). Les niveaux plasmatiques de GLP-1 actif (également sécrété par les cellules L) et de PYY atteignent le pancréas, où ils exercent un effet modulateur dans la sécrétion des hormones par les ilôts pancréatiques. (B). Dans les cellules β-pancréatiques, le glucose est métabolisé ; pour produire des molécules d’ATP à haute énergie, causant une augmentation du rapport ATP/ADP, fermant les canaux potassiques (K+ ATP) sensibles à l’ATP. Des niveaux élevés de potassium intracellulaire conduit à une dépolarisation de la membrane, qui, à son tour, ouvre les canaux calciques dépendant du voltage, augmentant ce faisant la concentration en ions calcium dans le cytoplasme. Cela stimule le relâchement de l’insuline à partir des vésicules de sécrétion. (…). La liaison du GLP-1 à son récepteur provoque une augmentation d’AMPc et une activation de la protéine kinase A ; l’inhibition des canaux K+ ATP, empêchent la repolarisation de la cellule β, sensibilisant également les canaux calciques du réticulum endoplasmique (ER) et permet le relâchement du calcium à partir des réserves intracellulaires, aidant à l’exocytose de l’insuline. L’engagement chronique du récepteur NPY1R par le PYY amplifie également par l’intermédiaire de mécanismes encore non-identifiés. (…). Dans les cellules α, le GLP-1 et le PYY stimulent la suppression du glucagon induite par le glucose par des voies de signalisation directes et indirectes qui restent à caractériser. (…).
La chirurgie bariatrique mène à une rapide et durable rémission du diabète de type 2 (T2D) chez les sujets obèses. Ce phénomène survient indépendamment de la perte de poids, probablement par le truchement d’une combinaison de facteurs. À date, on dit de l’hormone incrétine GLP-1 qu’elle représente un facteur critique, dans ce cadre. Cependant, de récentes données indiquent que l’élévation des taux d’une autre hormone intestinale, le Peptide Tyrosine-Tyrosine (PYY) pourrait représenter la force motrice des effets bénéfiques de la chirurgie. Ici, nous discutons des récentes découvertes relatives au contrôle de l’homéostasie glucidique par le PYY - ainsi que de son rôle dans le diabète, dans le contexte de ce que l’on connaît sur le GLP-1. L’identification de facteurs produisant l’augmentation de l’expression du PYY suivant une chirurgie bariatrique et l’élucidation de son rôle dans la suppression du diabète pourrait représenter un argument en faveur de son application dans le cadre d’une thérapie non chirurgicale du T2D. Claudia Guida, et al, dans Trends in Endocrinology and Metabolism, publication en ligne en avant-première, 19 mai 2017Source iconographique, légendaire et rédactionnelle: Science Direct / Traduction et adaptation : NZ
