Ici, les chercheurs du Centre RIKEN au Japon ont cultivé en laboratoire, avec succès, ce tissu complexe de la peau, avec ses follicules pileux et ses glandes sébacées. Les chercheurs sont partis de cellules de gencives de souris, les ont transformées en CSPi, qui se sont développées en corps embryoïdes, puis en tissu différencié, transplanté enfin chez les souris vivantes. Un élément important de ce processus est le traitement des cultures avec une molécule de signalisation, Wnt10b, qui permet le développement d’un nombre accru de follicules pileux, ce qui rend le tissu de bio-ingénierie plus proche du tissu naturel. Les tissus enfin transplantés ont formés les bonnes connexions avec les tissus, organes, nerfs et fibres musculaires environnantes.
Une nouvelle voir prometteuse pour des greffes de peau : c’est un espoir pour les grands brulés ou les patients qui ont besoin de greffes de peau. C’est aussi une nouvelle étape dans l’ingénierie de la peau, car si on est capable de développer des couches de cellules épithéliales implantables, elles ne disposent pas encore des appendices appropriés qui leur permettraient d’assumer l’ensemble des fonctions du système tégumentaire normal.
Jusqu’à présent, le développement par bio-ingénierie de peau artificielle était limité par le fait que la peau produite ne disposait pas de ses organes importants, tels que les follicules pileux et des glandes exocrines, qui permettent à la peau de jouer son rôle important dans la régulation.
» Avec cette nouvelle technique, nous avons développé avec succès une peau qui reproduit une grande partie des fonctions du tissu normal. Le défi est de parvenir, en laboratoire, à être de plus en plus proche des organes réels « , conclut Dr Selon Takashi Tsuji, auteur principal de l’étude.
Source: Science Advance 01 Apr 2016 DOI: 10.1126/sciadv.1500887 Bioengineering a 3D integumentary organ system from iPS cells using an in vivo transplantation model
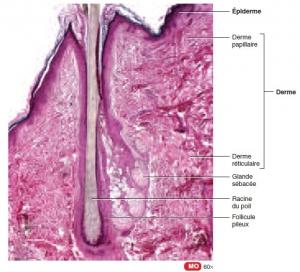
(Visuel « le système tégumentaire et l’homéostasie « @De Boeck)



