 Un moteur qui tourne trop vite, s’épuise, surchauffe et finit par casser. Cette image, une surchauffe de neurones spécifiques, impliqués dans le contrôle moteur, c’est l’explication des symptômes moteurs de la maladie Parkinson, documentée par cette équipe de l’Université de Montréal (UdeM). Les conclusions, présentées dans la revue Current Biology ouvrent la voie à une meilleure compréhension de la maladie et au développement de médicaments capables de calmer la surchauffe.
Un moteur qui tourne trop vite, s’épuise, surchauffe et finit par casser. Cette image, une surchauffe de neurones spécifiques, impliqués dans le contrôle moteur, c’est l’explication des symptômes moteurs de la maladie Parkinson, documentée par cette équipe de l’Université de Montréal (UdeM). Les conclusions, présentées dans la revue Current Biology ouvrent la voie à une meilleure compréhension de la maladie et au développement de médicaments capables de calmer la surchauffe.
Le Dr Louis-Éric Trudeau, professeur à l’Université de Montréal s’intéresse depuis 17 ans au fonctionnement d’une zone du cerveau impliquée dans la maladie de Parkinson, la schizophrénie et la dépendance aux drogues. Son obstacle, la difficulté à développer un modèle animal de la maladie : « Les laboratoires ne parviennent pas à reproduire chez la souris les symptômes de la maladie de Parkinson, même par modifications génétiques « , explique l’auteur qui voit aussi, dans sa découverte, le moyen de proposer des lignées animales mieux adaptées à la recherche.
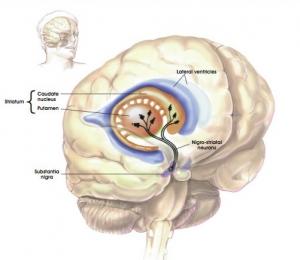
Depuis 3 années, l’équipe cherche à identifier les mécanismes en cause et à confirmer l’hypothèse de la » surchauffe » des neurones. Ces derniers travaux expliquent que les symptômes de la maladie de Parkinson sont causés par la mort de dizaines ou centaines de milliers de neurones dans certaines zones bien précises du cerveau dont la substance noire (locus niger), le locus ceruleus (Vignette) et le noyau dorsal du nerf vague. La surchauffe pourrait être causée par des cellules très complexes -comptant un nombre élevé de prolongements et de sites de libération de neurotransmetteurs (Visuel ci-contre)- et très vulnérables. Leur dysfonctionnement déclencherait la maladie de Parkinson : ces neurones très complexes, présents dans les zones citées plus haut, forceraient les mitochondries à travailler trop fort pour produire de l’énergie, ce qui induirait leur usure accélérée.
» D’un point de vue évolutif, certain de nos neurones ne sont pas programmés pour durer 80, 90 et même 100 ans. Il faut s’attendre à ce qu’une partie du système subisse plus difficilement les effets du temps », explique l’auteur. Et cela vaut pour l’ensemble des maladies neurodégénératives.
Cette nouvelle lumière sur ce processus de surchauffe qui conduit à la maladie, ajoute à sa compréhension bien sûr, mais pourrait aussi faciliter le développement de modèles animaux. Avec de meilleurs modèles animaux, c’est le développement de médicaments capables de » calmer » ces neurones et leurs mitochondries, qui devient possible aussi.
Source: Current Biology 27 août 2015 DOI: 10.1016/j.cub.2015.07.050 Elevated mitochondrial bioenergetics and axonal arborization size are key contributors to the vulnerability of dopamine neurons (Vignette et visual NIH)


