Le syndrome de l’X fragile, une cause héréditaire de l’autisme peut avoir des conséquences même pour les porteurs » légers » de l’anomalie qui présentent des symptômes plus subtils. Cette étude de l’Université de Washington (St. Louis) identifie une cible prometteuse pour traiter ces personnes porteuses d’une » version légère » de la mutation : Il s’agit d’une protéine, clé pour la plasticité cérébrale, mais qui dans ce cas, aggrave les effets de la mutation.
Chez les patients » X fragile « , le gène FMR1, présent sur le chromosome X, est complètement désactivé, ce qui prive le cerveau d’une protéine clé, FMRP qui régule des signaux électriques dans le cerveau. Cette anomalie entraîne un grand nombre de symptômes comportementaux, neurologiques et physiques. Un des mystères de ce syndrome est comment la perte d’un seul gène peut conduire à une telle variété de symptômes chez différents patients. Certains patients sont profondément handicapés mentaux, incapables de communiquer. D’autres ne sont que légèrement touchés. Les patients éprouvent souvent des convulsions, l’anxiété et une impulsivité. Le syndrome entraine également des symptômes physiques dont la tête élargie, les pieds plats et des traits du visage bien particuliers. Enfin, près d’un tiers des patients atteints de syndrome X fragile présentent également des symptômes de troubles du spectre autistique (TSA).
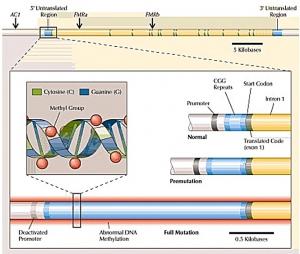
Différents niveaux de mutation dans le gène FMR1:
La mutation se produit lorsqu’une partie du code génétique est répétée à tort.
· Si la répétition erronée du code génétique se produit plus de 200 fois, cela bloque totalement la production de la protéine et entraine le développement du trouble à part entière avec ses symptômes lourds de déficits intellectuels et d’attention, d’hyperactivité, d’anxiété et de troubles de la communication sociale (Voir » Full mutation sur illustration ci-contre).
· Chez d’autres porteurs, la répétition erronée du code génétique dans le gène FMR1 est moindre et les symptômes sont alors plus subtils (Voir » Premutation « , sur illustration ci-contre).
Le double jeu d’une protéine clé : La recherche s’est focalisée autour d’une protéine au rôle particulier, Cdh1-APC suspectée d’être liée à la protéine de l’X fragile. La fonction principale de cette protéine est, en se liant à d’autres protéines dans le cerveau de les cibler pour les éliminer lorsque leurs fonctions ne sont plus nécessaires. Cdh1-APC joue donc un rôle clé dans le développement et la structure des réseaux de cellules du cerveau, elle affecte les synapses et, plus largement, les connexions entre les cellules nerveuses. Lorsque les chercheurs » éteignent » Cdh1-APC chez la souris, ils constatent que le processus de signalisation à travers les synapses est modifié.
Une question de plasticité : Cependant, si elle favorise la plasticité, Cdh1-APC interagit aussi avec la protéine de l’X fragile. Ici, les chercheurs identifient ainsi un segment dans la protéine de l’X fragile auquel Cdh1-APC s’attache et appose sa marque de destruction. Bloquer l’interaction entre Cdh1-APC et la protéine de l’X fragile permettrait de limiter la dégradation de la protéine, de rétablir ses niveaux et donc d’alléger certains des symptômes ressentis par les porteurs de cette maladie.
Source: Neuron April 23, 2015 DOI: 10.1016/j.neuron.2015.03.049 A Cdh1-APC/FMRP signaling link drives mGluR-dependent synaptic plasticity in the mammalian brain
(Visuel@National Fragile X Foundation)


