 Le poisson zèbre nous en apprend avec cette recherche expérimentale de l’Ecole de médecine Perelman sur la neurofibromatose, une des maladies neurologiques héréditaires les plus fréquentes, qui touche environ une personne sur 3.000. Les conclusions, présentées dans la revue Cell Reports, identifient 2 voies distinctes impliquées dans les déficits d’apprentissage et de mémoire typiques de la maladie. 2 cibles donc pour un futur traitement.
Le poisson zèbre nous en apprend avec cette recherche expérimentale de l’Ecole de médecine Perelman sur la neurofibromatose, une des maladies neurologiques héréditaires les plus fréquentes, qui touche environ une personne sur 3.000. Les conclusions, présentées dans la revue Cell Reports, identifient 2 voies distinctes impliquées dans les déficits d’apprentissage et de mémoire typiques de la maladie. 2 cibles donc pour un futur traitement.
La neurofibromatose (NF1) qui se caractérise par des tumeurs le long des nerfs entraine des déficits de l’attention et des troubles de l’apprentissage. La plupart des patients atteints présentent leurs premiers symptômes avant l’âge de 10 ans. Les traitements vont cibler une famille de protéines (Ras) impliquée dans la prolifération cellulaire. Le gène NF1 code pour la neurofibromine, une protéine dont un petit domaine participe à la régulation de Ras.
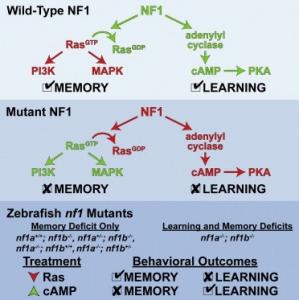
Cibler spécifiquement les « voies » de l’apprentissage et de la mémoire apparait ainsi comme une stratégie plus efficace, selon le Dr Jon Epstein, président du département de biologie cellulaire et développementale de l’Université, l’un des auteurs de l’étude : « Les troubles de la mémoire sont liés à une activité anormale de Ras, les déficits d’apprentissage ne sont pas affectés par la modulation de ces mêmes voies ». Ces nouvelles données suggèrent également que ces déficits d’apprentissage et de la mémoire typiques de NF1 sont réversibles, avec des traitements pharmacologiques et ne sont donc pas figés par un défaut dans le développement des nerfs.
Un grand espoir donc pour les patients atteints de NF1.

