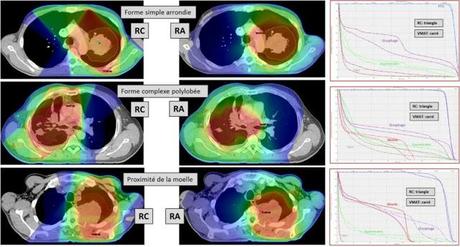
Distribution de dose en radiothérapie conformationnelle (RC) et en RapidArc TM (RA) (VMAT) dans trois situations cliniques différentes. In Cancer/Radiothérapie Volume 16, Issue 7, October 2012, Pages 619 - 626
Source iconographique et légendaire: http://www.sciencedirect.com/science/article/pii/S1278321812003824
Le paramètre de référence, mesuré lors d’essais cliniques de chimiothérapie et de radiothérapie dans le cancer du poumon, reste la survie globale. Bien que fiable et simple à mesurer, ce paramètre prend des années à mesurer. Des critères de substitution qui permettraient des évaluations de traitement plus précoces, seraient très utiles. Nous avons étudié les corrélations existant entre les critères de substitution et la survie globale au niveau du patient pris individuellement, et au niveau global de l'essai. Nous avons analysé les données individuelles provenant de 15 071 patients engagés dans 60 essais cliniques randomisés faisant l'objet de six méta - analyses. Deux méta – analyses portaient sur la chimiothérapie adjuvante dans le cancer du poumon non à petites cellules, trois portaient sur des chimiothérapies administrées de manière séquentielle ou concomitante, et une portait sur la radiothérapie dans le cancer du poumon localement avancé. Nous avons étudié la survie sans récidive (DFS), la survie sans progression de la maladie (PFS) [définie par le temps écoulé entre la randomisation et une rechute locale ou à distance, ou le décès du patient], ainsi que le contrôle locorégional [défini par le temps t d’occurrence du premier événement local] comme paramètres de substitution. Au niveau individuel, nous avons calculé les corrélations au carré entre les distributions obtenues sur ces trois paramètres mesurés et la survie globale ; et au niveau de l’essai, nous avons calculé les corrélations au carré entre les effets des traitements comme critères d’évaluation.
Dans les essais de chimiothérapie adjuvante, les corrélations entre la DFS et la survie globale étaient très bonnes à un niveau individuel (p2=0,83 ; Intervalle de Confiance – IC – 95% 0,83-0,83 dans les essais sans radiothérapie ; et 0,87 ; 0,87-0,87 dans les essais avec radiothérapie) et excellentes au niveau de l’essai (R2 = 0,92 ; IC 95% 0,88-0,95 dans les essais sans radiothérapie et 0,99 0,98-1,00 dans les essais avec radiothérapie). Dans les études portant sur une pathologie localement avancée, les corrélations entre PFS et survie globale étaient très bonnes au niveau individuel (0,77 ≤ p2≤ 0,85 ; dépendant du traitement à l’étude) et au niveau de l’essai (0,89 ≤ R2 ≤ 0,97). Dans les études avec données de contrôle locorégional, les corrélations à un niveau individuel étaient bonnes (p2=0,71 ; IC 95% 0,71-0,71 pour la chimiothérapie concomitante; et p2=0,61 ; 0,61-0,61 pour la radiothérapie modifiée versus radiothérapie standard); et les corrélations au niveau de l’essai très bonnes (R2=0,85 ; IC 95% 0,77 – 0,92 pour la chimiothérapie concomitante et R2=0,95 ; 0,91-0,98 pour la radiothérapie modifiée versusradiothérapie standard).
De nombreux et solides indices montrent que la DFS est un critère de substitution valide pour l’évaluation de la survie globale dans les études de chimiothérapie adjuvante impliquant des patients atteints de cancer du poumon non à petites cellules, et la PFS dans les études de chimiothérapie et de radiothérapie effectuées chez des patients atteints de cancer du poumon localement avancé. L’extrapolation à d’autres agents thérapeutiques et cibles n’est pas automatiquement recommandée. Audrey Mauguen, MSc et al, in The Lancet Oncology, Early Online Publication, 14 May 2013
Financement: Programme Hospitalier de Recherche Clinique, Ligue Nationale Contre la Cancer, British Medical Research Council, Sanofi-Aventis
Source : The Lancet Online / Traduction et adaptation : NZ
