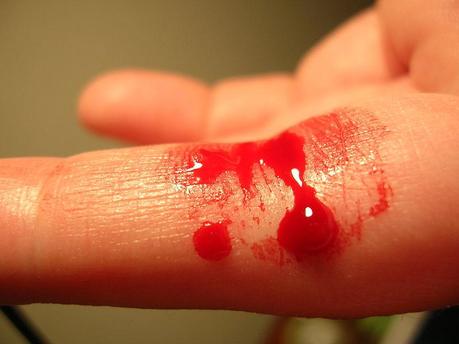
 Saviez-vous que Peter Jackson avant de réaliser le Seigneurdes anneaux fut un réalisateur de film gore à très petit budget ? (Voir parexemple "Braindead" ou "Bad Taste"…) Autrefilm bien adapté à notre sujet du jour: "Sweeney Todd, le diaboliquebarbier de Fleet Street" de Tim Burton. Et que dire encore de la série Dexter,où le personnage principal est un expert de l’analyse des tâches de sang etégalement un tueur en série. Vous l'aurez deviné, notre sujet du jour est le sang. Star des films d’horreur, sa couleur rouge vif met nos sens enalerte, et suffit à faire détourner le regard des plus sensibles (C’estd’ailleurs pour cela que les orcs ont le sang noir et non rouge dans le Seigneur des anneaux : on éviteainsi l’interdiction du film au moins de 12 ans ...). Mais à quoi est due cettecouleur si intense ? Et pourquoi le sang non oxygéné des veines est-iltoujours représenté plus sombre ou plus bleu que le sang oxygéné desartères ?
Saviez-vous que Peter Jackson avant de réaliser le Seigneurdes anneaux fut un réalisateur de film gore à très petit budget ? (Voir parexemple "Braindead" ou "Bad Taste"…) Autrefilm bien adapté à notre sujet du jour: "Sweeney Todd, le diaboliquebarbier de Fleet Street" de Tim Burton. Et que dire encore de la série Dexter,où le personnage principal est un expert de l’analyse des tâches de sang etégalement un tueur en série. Vous l'aurez deviné, notre sujet du jour est le sang. Star des films d’horreur, sa couleur rouge vif met nos sens enalerte, et suffit à faire détourner le regard des plus sensibles (C’estd’ailleurs pour cela que les orcs ont le sang noir et non rouge dans le Seigneur des anneaux : on éviteainsi l’interdiction du film au moins de 12 ans ...). Mais à quoi est due cettecouleur si intense ? Et pourquoi le sang non oxygéné des veines est-iltoujours représenté plus sombre ou plus bleu que le sang oxygéné desartères ?


Du sang à l’hémoglobineQue contient le sang ? Et bien sion centrifuge le sang on distingue 3 fractions : le plasma plutôt jaune,c’est la portion liquide du sang, elle correspond à 55% du sang total, lesglobules blancs et plaquettes (moins de 1%) et enfin les célèbres globulesrouges appelées hématies chez l’Homme qui correspondent à 45% du volume total (Ce pourcentage s’appelleégalement hématocrite, sur une analyse de sang).
Ces hématies donnent leur couleur rouge au sang, ce sontdes cellules sans noyaux et pratiquement sans organites, elles contiennent pourl’essentiel une seule protéine : la fameuse hémoglobine. Ces sacsd’hémoglobine ont pour mission de transporter l’oxygène dans tout l’organismegrâce à cette protéine aux propriétés remarquables (Je suis sûr que tous les amateurs du fameuxdessin animé « Il était une fois... la Vie» s’en souviennent).
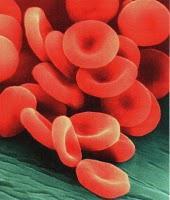
 [Les hématies en microscopieélectronique à balayage (fausses couleurs) et selon le dessin animé « Il était une fois... la Vie » (Albert Barillé - 1987).]
[Les hématies en microscopieélectronique à balayage (fausses couleurs) et selon le dessin animé « Il était une fois... la Vie » (Albert Barillé - 1987).]La structure de l’hémoglobineLa protéine est composée de 4sous-unités protéiques, les globines: deux α etdeux β, chaque sous-unité étant liée à ungroupement non protéique, l’hème ; d’où le nom :« hémo-globine ». Cet hème contient un atome de Fer lequel peut selier avec la molécule de dioxygène. Chacune des millions de moléculesd’hémoglobine d’un globule rouge peut donc transporter 4 molécules de dioxygène.L’emplacement réservé pour le dioxygène, n’est pas utilisé pour transporter ledioxyde de carbone (CO2), par contre le monoxyde de carbone (CO) est suffisamment petit pour venir se fixer defaçon quasi-irréversible sur ce site. Comme la place de l’O2 est prise, lemanque d’oxygène se fait vite sentir même pour de faibles concentrations en CO…C’est l’origine des empoisonnements au monoxyde de carbone souvent liés à devieux poêles et autres chaudières mal réglées.
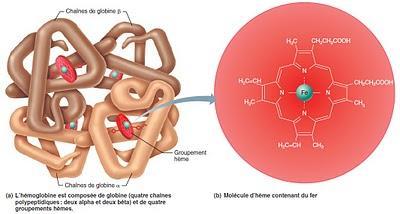 [L’hémoglobine : une protéine àstructure quaternaire, c'est-à-dire composée de sous-unités. (2α et 2β)]
[L’hémoglobine : une protéine àstructure quaternaire, c'est-à-dire composée de sous-unités. (2α et 2β)]Une couleur variable selon le degréd’oxygénation.En absence d’O2 fixé sur l’hémoglobine,l’atome de fer II (fer ferreux) lié par une liaison faible à un acide aminé(l’histidine) est décalé par rapport au plan de l’hème. Il dépasse un peu comme s’il était tiré sur le coté par sa liaison avec l’histidine. De plus la répartition des électrons autour du noyau fait que le diamètre global de l’atome est important. On parle de configuration Bas spin. A l’inverse lorsque le dioxygène se fixe sur l’atome de fer du coté opposé à celui de l’histidine, il prend une position parfaitement centrée par rapport au plan de l’hème, et son diamètre est réduit : on parle de configuration Haut spin.Cettesimple différence entre la configuration Haut spin et Bas spin et les changements qui l'accompagnent, suffisent à créerune différence importante dans le spectre d’absorption de la molécule, autrementdit, sa couleur. Ainsi l’oxyhémoglobine absorbe beaucoup moins dans lescouleurs d’onde du rouge (env. 660nm) que la désoxyhémoglobine, qui apparaît donc moinsrouge. Son aspect est plus terne, plus proche du bleu, et voilà la raison decette représentation conventionnelle du sang non oxygéné en bleu et du sangoxygéné en rouge.
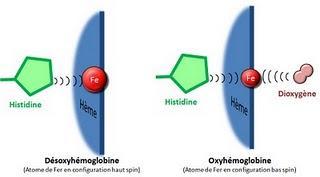
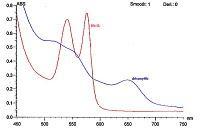 Ci-dessus:[A gauche: Configuration et position de l'atome de fer dans le plan de l'hème dans le cas de l'oxy. et de la désoxyhémoglobine. A droite: Le spectre d’absorption del’hémoglobine oxygénée et non oxygénée, mesuré lors d’un TP de physiologieanimale de L3 (UPPA). La désoxyhémoglobine (en bleu) absorbe beaucoup moins dans le rouge (660nm) que l'oxyhémoglobine (en rouge).]
Ci-dessus:[A gauche: Configuration et position de l'atome de fer dans le plan de l'hème dans le cas de l'oxy. et de la désoxyhémoglobine. A droite: Le spectre d’absorption del’hémoglobine oxygénée et non oxygénée, mesuré lors d’un TP de physiologieanimale de L3 (UPPA). La désoxyhémoglobine (en bleu) absorbe beaucoup moins dans le rouge (660nm) que l'oxyhémoglobine (en rouge).]L’hémoglobine, qualifiée de pigmentrespiratoire à cause sa couleur, n’est pas la seule molécule à assurer cettefonction de transporteur d’O2 dans le monde animal. Ainsi chez les crustacés ouchez les mollusques, on trouve l’hémocyanine, qui comprend deux atomes decuivre. L’atome de cuivre oxydé donne alors une couleur bleu-verte au sang. Sansdoute les orcs du Seigneur des anneaux ont-ils également une hémoglobinespécifique qui n’utilise pas le fer… Je propose le manganèse, à l’origine decertains colorants noirs. Pour finir sur une note moins triviale, sachezque l’hémoglobine constitue un remarquable outil de phylogénie moléculaire chez lesgnathostomes (vertébrés possédant une mâchoire).
[Retour à l'accueil]

